티스토리 뷰
2치전지 리튬이온배터리의 구조 및 작동 원리
일상생활에서 떼놓을 수 없는 스마트폰이나 각종 노트북, 무선 블루투스 이어폰과 태블린 PC 등 요즘은 전자기기와 삶이 매우 가까워진 시대입니다. 이러한 대부분의 무선 전자제품 안에는 2차전지인 리튬배터리가 탑재되어있는데요.
배터리 혁명에서 이제는 주류 배터리로 자리하게된 이차전지 리튬이온배터리의 구조와 작동 원리에 관해서 간단히 알아보겠습니다.
2차전지 리튬배터리의 작동 원리
리튬이온배터리는 리튬 이온이 양극재와 음극재 사이를 이동하며, 화학적 반응으로 전기를 생성해내는 방식으로 작동하게 됩니다. 양극 리튬 이온이 음극으로 이동하면 배터리가 충전되고, 음극에서 양극으로 이동하면 배터리를 소모하며 에너지를 방출해냅니다.
리튬 이온이 양극재와 음극 사이를 이동하려면 이동통로가 필요한데, 이 이동통로 역할을 하는 것이 바로 전해질입니다. 또, 전해질과 양극 / 음극이 서로 닿지않게 막아주는 분리막이 필요합니다.
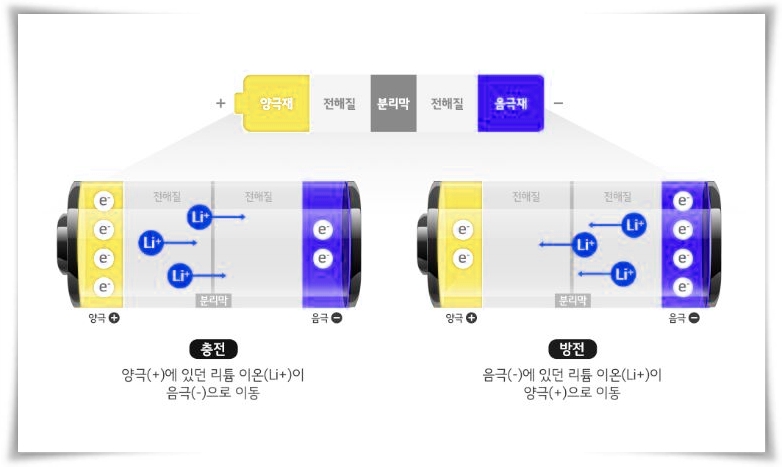
이렇게 양극재, 음극재, 전해질, 분리막 4가지가 총칭 리튬이온배터리의 4대 구성요소입니다. 이 4대 구성요소가 각각 하는 일을 알아보겠습니다.
리튬배터리의 4대요소
양극재 / 음극재 / 전해질 / 분리막
원소상태의 리튬은 불안정하여 산소와 결합하여 리튬 산화물 형태로 양극에 들어갑니다. 이 리튬산화물이 들어가는 공간이 바로 양극재라고 할 수 있으며, 리튬의 성질 자체가 전자를 잃고 양이온이 되려는 성질이 강하기 때문에 양극소재로 적합합니다.
양극재 리튬의 비중이 높을수록 배터리 용량이 커지게 되며, 효율성을 위해 최근 NCA, NCMA등의 다양한 종류의 양극재가 개발 및 상용화되는 추세입니다.
음극재는 양극에서 나오는 리튬 이온들을 저장하고 방출하며, 회로에서 전류가 발생하게 만듭니다. 배터리를 충전하고 있는 경우, 리튬이온은 음극에 존재하며 도선을 통해 리튬이 양극으로 이동하게 하면, 리튬에서 전자가 분리되어 도선을 흐르며 전류를 만듭니다.
음극재에 가장 많이 사용되는 재료는 흑연이며, 흑연은 이온 저장을 가장 안정적으로 할 수 있는 물질 중 하나입니다. 허나 리튬이온의 저장과 방출이 반복되면서 흑연의 구조가 점점 변화하게 됩니다. 이렇게 흑연의 구조가 변화할수록 저장할 수 있는 이온의 양이 감소하게 되는데, 이것이 배터리를 사용할수록 배터리수명이 줄어드는 이유입니다.
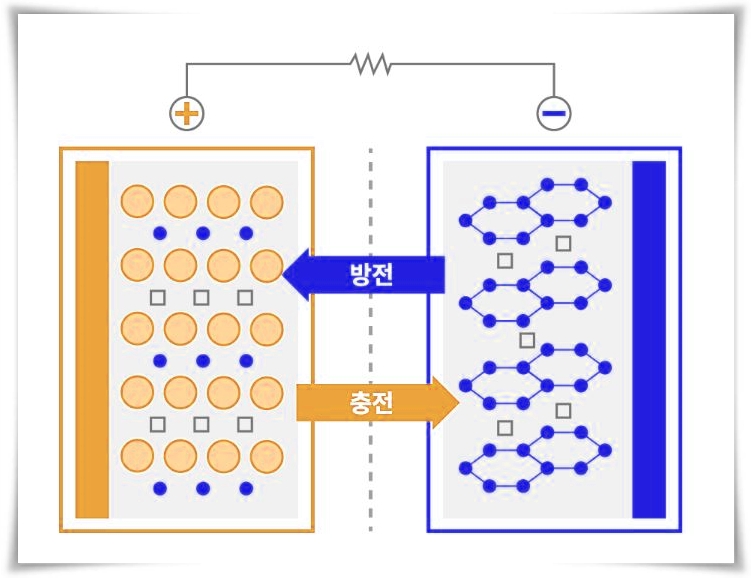
분리막은 이온이 이동할때 양극과 음극이 물리적으로 접촉되는 것을 방지하며, 주로 전기절연성과 열안정성이 높은 PE / PP 재질이 사용됩니다. 일반적으로 전선의 피복 재질을 생각하면 됩니다.
전해질은 배터리 내부에서 리튬의 이동을 원활하게 해주는 매개체라 할 수 있으며, 이온 전도도가 높은 물질이 사용됩니다. 또한 화재 및 안전사고 방지를 위해 높은 발화점이 요구됩니다. 현재 상용화된 대부분의 전해질은 액체 형태이며, 최근에는 고체 및 젤형태의 전해질 연구도 진행되고 있습니다.
'이슈 & 잡다한 정보' 카테고리의 다른 글
| 개업화분 선물 - 돈들어오는 나무, 화초, 식물 종류 (0) | 2023.01.03 |
|---|---|
| 선물용 만년필 브랜드 종류 순위 BEST 5 (1) | 2023.01.02 |
| 아기로션 순위 / 베이비로션 추천 모음 BEST 5 (0) | 2022.12.24 |
| 어서와 한국은처음이지 - 최고급 한우 퓨전 코스요리 (0) | 2022.12.24 |
| 거실, 침실용 러그 / 카펫 브랜드 추천제품 모음 (0) | 2022.12.22 |
